氮循环是全球生物地球化学循环的重要组成部分,也是生物圈内基本的物质循环之一。自然界中的氮绝大部分以氮气分子(N2)的形式存在于大气中。N2的化学性质不活泼,常温下很难与其他物质发生反应。此外,大部分生物体无法利用N2进行新陈代谢。因此,N2需要被转化为“活性”氮(如NH3-N),才能被广大生物体所利用。将N2转化为“活性”氮的过程称为固氮作用,通常由微生物(包括细菌和古菌)完成,此外,20世纪初发明的Haber-Bosch固氮法是一种得到了广泛应用的化学固氮法。
( {+ V$ Q! q3 H& V2 Z, L1 ^8 T* M- P' H, {( U0 L$ K- z
1 @! q. `7 l" ?, s5 \
得益于工业和农业的快速发展,人类的物质生活水平得到了极大的提升。但是同时,全球每年通过工业、农业等活动向环境中排放大量含氮废水,使自然水体中新增越来越多的“活性”氮,导致日渐严重的氮循环失衡问题。据统计,人类每年向环境中排放的氮总量约为2000多万吨,并且这个数字随着人口的增长在不断攀升。更糟糕的是,大约一半的氮污染物没有经过处理,被直接排放至环境中。+ n- g+ M/ Q4 F; s4 h" O. m( L) _
" b/ v7 \4 o4 L" P' P* e+ P. c2 H# O例如,在发展中国家,超过35%的城市没有污水处理厂(WWTP)。即使在拥有WWTP的城市,一部分WWTP对污水只进行初级处理,脱氮能力非常有限。这一系列问题对水体中氮循环的影响主要包括:+ W- J( c; I2 F
& M2 v6 G$ L9 C4 S# m
流域内氮沉积能力下降;
3 @$ m1 F1 J0 P4 n$ ?$ a, j" ]6 W$ S( f- {# S+ B) [4 t4 _
水体中氮素排放量增加。具体而言,这造成了水体富营养化、水体酸化和温室气体排放等一系列环境问题。
4 M, D+ f7 n7 L- k; e6 q6 M/ S" @, x4 I/ h8 I: r' Q& W% O
污水中氮的主要形态及转化
7 a; i: b" K, u( ?7 G$ H: @5 [5 J3 j' n/ l8 W) u
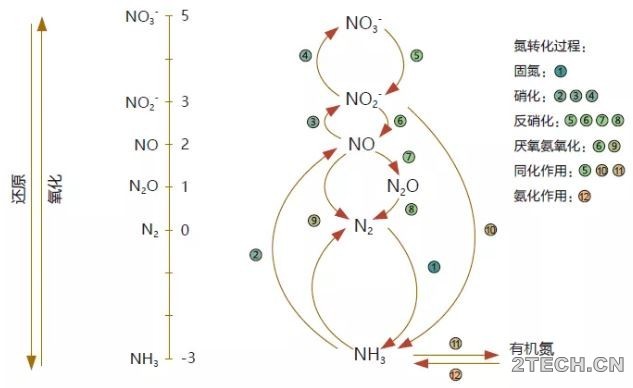
市政污水通常是工业废水、生活污水和径流污水的集合体。市政WWTP进水中的氮主要包括NH3和有机氮。氮的循环转化过程主要包括同化吸收、氨化、硝化、反硝化、厌氧氨氧化和固氮(图1)。0 p- D$ L: T* n. M$ I
4 H) g7 V, u; b+ p4 Z
8 [3 W8 o# c' t" M
* G/ F9 u6 X2 f" Y; u! y+ [7 [图1 氮循环过程
( d& ]1 L' W& J! o% d+ k! L1 e: P* `+ y$ z% c4 N
氨氮(NH4+或NH3)# D; H3 _( @8 p+ u, J7 p& h% y
3 ~$ q0 u6 b6 L9 b7 S, g0 k
氨氮的浓度在不同类型的污水中差异非常大。在市政污水处理厂的进水中,氨氮的浓度通常介于20 ~75 mg-N/L 。污水中NH3的主要来源包括:# t) g4 w6 a5 |
- `: K# b) v# [4 I5 W有机氮的降解,如蛋白质降解为NH3;. |0 w3 l* W/ ?! i
0 |% j$ F: g! r1 m3 o# Q
固氮作用,例如微生物固氮作用以及Haber-Bosch固氮法;
: w {) H) v; o3 L8 d5 r
; H) ]* `. w1 C6 v亚硝酸盐(NO2-)的还原,它在氮的异化和同化过程中都存在。
& e7 u" s/ @7 f! {# h2 y
+ s; F4 p0 b/ ?$ z' t4 @在污水处理过程中,脱除NH3的主要方式是将其氧化为N2或NO2-。其中,后者的转化过程是通过中间产物一氧化氮(NO)来实现的。. P/ j e6 ]8 {+ r& w
3 f- K; K$ q q: E& D4 p4 v
亚硝酸盐(NO2-)2 X# a# X8 }3 j8 R0 c5 d
4 P4 b9 ]$ _2 b+ j. Q; x+ H4 |7 _" h, S
与NH3相比,污水中NO2- 的含量通常比较低。NO2- 的形成主要是由于NH3的氧化或NO3- 的还原。NO2- 的去除可以通过将其氧化形成硝酸根(NO3-),或者还原形成N2或NH3。其中,在将NO2-还原成N2的过程中,有中间产物NO生成。在NO被进一步还原为N2的过程中,有氧化亚氮(N2O)产生。N2O是一种强效的温室气体,其温室效应是CO2的三百倍左右。污水处理过程中N2O的释放是近年来受到关注的领域之一。9 R t2 j4 ~+ k& [
# M/ \5 c N1 \' o硝酸盐(NO3-)
: T# u2 r/ [" o8 s/ k' i! ^, R$ Y/ n% ^3 |
NO3-是含氮有机物氧化分解的最高价态化合物。污水中的NO3-是由于NO2-的氧化而形成。NO3-的去除可通过将其还原为NO2-而实现。由于人类活动的影响,许多地方的地下水和地表水中NO3-含量在不断升高,造成了越来越多的土壤和地下水质量安全问题。9 T# A3 s6 p6 g; n
* u7 n: Z* j' Q! w有机氮) W. @2 W0 j/ i8 c3 L9 E f
y" _# P. y3 R9 V. k
污水中的有机氮主要是蛋白质,此外还有尿素、胞壁酸、脂肪胺、尿酸和有机碱等含氨基和不含氨基的化合物。有机氮的主要来源包括炼油、皮革、化肥、肉类加工和饲料生产等行业排放的废水。在污水贮存或在排水管道中停留一段时间后,氮的脱氨基反应使得有机氮转化为氨氮(NH3),导致NH3的浓度增加。
- Q- N0 y" H* A+ p( f d" M% t3 F0 ?1 \# Q8 C8 `6 V. S, a7 q
污水脱氮技术工艺# W5 r W7 t5 f
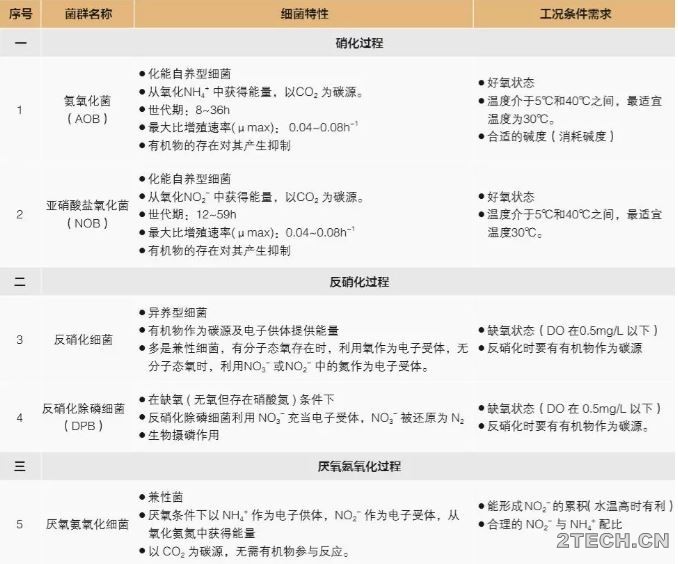
$ c8 L* d. u6 c8 B S3 N3 m从20世纪80年代开始,污水脱氮受到越来越多的关注。在传统的污水处理过程中,氮被转化为N2从而从污水中得到脱除。脱氮的过程通过各种微生物菌群来实现,相关的微生物菌群如表1。氮的脱除是一个高耗能、且昂贵的过程。随着城市化和人口的进一步增长,以及对水质要求的不断提升,对氮进行处理的要求也在不断提高。近几十年来,研究人员和工程师在探索污水生物脱氮的路上不停前行,不但致力于提高氮的脱除效率,而且追求降低处理过程中的能耗、环境足迹和处理成本。2 f9 G$ P4 m: ?% n
0 a1 p( H; W5 K& u1 t6 l表1 生物脱氮除磷菌群及特性
. T$ a9 E( V1 \7 C7 u
6 C+ @/ i9 O0 J9 n/ @
7 x* l g5 | E* w, k+ T" J1 z; q2 I0 B! y; U
硝化/反硝化
$ t: }: S# }, K4 s6 r5 a6 D
7 W6 k/ ?# n9 o6 @! `将NH3氧化成NO3-叫硝化,将NO3-还原成N2叫反硝化。污水中的NH3可以通过硝化和反硝化生成N2从污水中脱除,这是最早和最流行的污水生物脱氮技术。成功实现这个技术的前提是,污水中存在足够的氧气(O2)和有机物(可以换算成化学需氧量,即COD)。
& A) }2 M& N3 F4 R; d& ~/ j6 k8 o( ~* t; f% d3 c
在实际运行过程中,通常需要向污水中大量供氧,这是一个极其耗能的过程。此外,市政污水中含有的COD常常无法满足脱氮过程的需求,因此,需要向污水中补充额外的COD,这进一步提高了污水处理成本。更重要的是,由于硝化菌的生长速度缓慢,完成硝化过程需要足够的生物量停留在水处理反应器中,所以硝化过程需要占用的体积比非常高。+ g9 p, }9 }: S: J- n
% A! C. x6 w8 C3 e
Sharon新工艺! W$ {7 y! Q! b
& H& K7 g4 D& a' a& |, H! {由于传统的硝化和反硝化脱氮工艺的高成本与高能耗,科学家们一直在持续探索新的脱氮工艺,以提高污水生物脱氮过程的可持续性。在上世纪90年代,荷兰代尔夫特理工大学的科学家报道了一个新的工艺,名字叫Sharon(Single reactor system for High activity Ammonium Removal Over Nitrite缩写)。顾名思义,Sharon工艺是通过将NH3氧化成NO2-之后,再将NO2-还原成N2的过程,整个工艺可以在一个反应器内完成。
; ~% u: i4 i. u0 s: w3 p1 r/ M- s. G, L3 w6 ` K, C: @: G& a
Sharon工艺的第一次实际应用是在荷兰鹿特丹Dokhaven的污水处理厂。与传统的硝化/反硝化相比,Sharon工艺省去了将NO2-氧化为NO3-的过程。因此,它有明显的优势:$ A: O; v" G% w; {6 C: x }1 w0 W
* g: N- i2 t0 z
耗氧量减少,因此能耗减少;4 K$ b! h# ^4 u8 Q( w
/ a3 Z9 H0 ^1 J( p5 D" g
需要添加的COD量减少;# E5 O! o/ N: y }
) Q' z7 Y* }: W$ F. w, c整个过程可以在一个反应器内完成;# P A5 j" m# V( d) \- B! @* u
/ T- e. \& D! j; h不需要污泥停留。这些特点意味着,它能够有效降低污水生物脱氮的成本。
+ }! ^; a3 b7 U; ] f' e. J3 g9 _5 W( x3 o# }2 A) W+ _8 ~( n
厌氧氨氧化(Anammox)
\$ J y" }, ]& }
0 l4 V* s$ E9 ~7 Z5 p* J$ H3 ?除Sharon工艺外,科学家们发现了另一个生物脱氮过程,即厌氧氨氧化(Anammox)。在1977年,有科学家通过热力学计算,预言了Anammox的存在。直到1992年,这个预言得到了完全的验证和专利保护。简单来说,Anammox可以将NO2-作为电子受体、NH3作为电子供体,反应生成N2。2 |+ w$ a: i" W3 o) q$ R2 b
) B* Y# B: m3 d a' |+ ?
Anammox的主要特点包括:
+ z# d9 [* U: o
+ t7 H# Z" n* {) X反应的吉布斯自由能比O2介导的NH3氧化反应更低(见表1),因此从热力学的角度来说,Anammox更容易发生;
9 x) c }" A4 c6 U- E( q
n$ F# M3 ]$ \4 a' k$ z# d9 y7 M# _# |Anammox菌的生长速度较慢,倍增时间为3星期。5 k* a* E) B. q
# ~: T' X9 a, a: W; N因为Anammox具有这些特点,所以Anammox工艺的起始阶段耗时较长,运行Anammox工艺的反应器需要有很好的污泥停留能力。不过,它的优势也非常明显,与传统的硝化/反硝化工艺相比,Anammox的耗氧量减少60%,对COD的需求量减少100%,产泥量减少90%。
! L) R1 s$ g) P: V) z5 t+ e2 {7 L' b
短程硝化/厌氧氨氧化: f- r( r" ?3 ^8 r% a4 ^) @
- z2 ]' \, _; f
值得一提的是,Sharon和Anammox都是由荷兰代尔夫特理工大学的科学家最先报道,这是他们在执行荷兰应用水研究项目基金(the Dutch Foundation of Applied Water Research)时取得的研究成果。他们在研究的过程中发现,若将Sharon与Anammox进行联用,将50%的NH4+氧化为NO2-,再将这部分NO2-与剩余的NH4+反应生成N2,可以实现完全脱氮,这个过程称为Sharon/Anammox。在研究早期,通常使用两个反应器串联来分别实现Sharon和Anammox。目前,这个过程通过在一个反应器中操作完成,例如使用颗粒污泥或者膜生物反应器,使Sharon和Anammox分别在同一个反应器中的好氧和缺氧微环境中实现。, Y+ V: r, k; Q3 u. n& }
$ |8 ^6 ~( d. N8 |' A% _8 u- L% [
% _8 a! o1 s6 @' K, y! TSharon/Anammox工艺的优点包括:可以将耗氧量降低40%,达到节能效果;不再需要额外的COD,降低了成本;只有极小的产泥量,产生较少剩余污泥。
' S+ I$ ]% G+ Z }
6 I& W# @; W9 z# ~2 E' L% l由于Sharon/Anammox工艺在提升污水处理厂脱氮性能方面具有极大的应用前景,近十几年来,许多科学家和工程师投身于该技术的实际应用中。截至2014年,该工艺已经在超过100家WWTP得到应用,大部分在欧洲的WWTP,基于侧流Sharon/Anammox的技术在北美比较受欢迎。
0 G5 I' B: g* l1 E- a; q- e+ F/ }1 c7 z) C6 p% X
其他脱氮技术
% ^, J. u# V p$ r0 O/ a4 T I( V7 m" A. g" [) W
在进一步尝试将主流Sharon/Anammox应用于WWTP时,该工艺遇到了以下问题或技术瓶颈:
2 i0 j: W- Z! ~+ `- d v0 _# ~) D0 g& h6 N3 h
污水中COD与氮的比例太高,使异养菌过量生长;
% `- `# [" Z' y- e& C
6 n$ F0 R8 w4 n/ f3 T# w' O9 tNH3浓度太低,限制了Anammox菌和NH3氧化菌的生长;
- z( {# o5 H, |/ l/ ~' |( B& l, T: U: W3 @: L: i! I
污水温度太低,这意味着,与Anammox和NH3氧化菌相比,NO2-氧化菌容易获得生长优势;
* G) E+ [5 |# L- G
% U% ~! K6 O/ M: Z; j! k出水NH3浓度很难达到出水水质要求。
p$ N& }4 Z0 _4 E: s- a3 P" q2 u$ y" H3 s2 l4 V
由于这些技术瓶颈的存在,目前,主流Sharon/Anammox只在奥地利Strass和新加坡Changi共2家WWTP得到实际应用。它的大规模应用仍有较长的路要走。值得期待的是,研究人员正在尝试或者考虑尝试其他技术来突破这些技术瓶颈,例如:. s. J8 h+ V3 J- t- {* [) y0 T# ~
0 K5 V3 i) G9 Z! n% z3 y使用NH3氧化古菌为Anammox提供NO2-:与氨氧化细菌相比,氨氧化古菌对O3和NH3有更强的亲和力,因此可能有助于降低出水NH3浓度。
* j( D' A4 U% ?) ]4 Y
) Y7 `" f* M% ~& z使用反硝化型甲烷氧化菌(Damo):Damo可以将NO3-还原为NO2-,将Damo与Anammox联用,可能有利于稳定地为Anammox提供NO2-,从而降低工艺运行过程中对NO2-氧化菌进行抑制的要求。7 ?* t) s0 O! _& G" e( \- y4 d
( [) X2 {% C% c5 N5 b5 r基于不同电子受体的Anammox:研究发现,Anammox可以利用SO42-、锰或Fe3+作为电子受体,对NH3进行氧化,这可能意味它们有替代NO2-作为电子受体,应用于污水脱氮的潜力。
/ O9 J3 R3 _$ d4 ?! y8 j8 I q% }2 n
硫酸盐还原/自养反硝化/硝化耦合技术(SANI):这项技术首先将污水中的硫酸盐还原为硫离子(S2-),同时去除了COD;其次,利用硝化作用将污水中的NH3转化为NO3-,最后将S2-作为电子供体、NO3-作为电子受体将氮以N2的形式从污水中脱除。该技术在含高浓度硫酸盐的污水中可能有较好的应用前景。目前,此项技术在香港得到了成功应用。2 I) D0 ~" z6 x/ g; v) x
0 x4 T8 U5 ~, e; d+ \5 Q污水中氮的资源回收
! R, v" {* J+ \" b G9 W* O' a. Y4 p. D/ g+ z
氮本身是一种资源,例如它是氮肥和蛋白质的重要组成成分。在污水脱氮技术得到发展与应用的同时,污水中的氮越来越广泛地被认为是一种潜在的资源。近年来,越来越多的研究人员致力于开发污水中氮资源回收技术,其中有一定潜力的方向包括肥料(气体NH3,(NH4)2SO4,鸟粪石等)、饲料与食物蛋白。
0 }" X3 R5 F. O0 C7 S M( p3 b
6 ^6 ^# K7 R% I' I9 f0 p气体NH3:可以从含高浓度氨氮废水中分离出来,作为一种资源进行回收。目前,最受关注的NH3回收法包括通过吹脱法或电化学法从含高浓度NH3的废水中获得气体NH3。' R7 p* o2 z A5 z; a$ @
1 \0 c4 g' G% i% S* b) m8 |7 o(NH4)2SO4:将气体NH3通入硫酸溶液中,从而在较高温度下(如70ºC)生成硫酸铵。硫酸铵可以作为农业生产中的肥料,提供硫和氮等营养物质。目前,这项技术的实际应用非常少,在荷兰Zutphen的污泥脱水项目中得到了成功应用。
4 N* ~8 [" [) }' P6 j2 A: b" l1 Y' }0 K, J% c. G$ l# N
鸟粪石:将镁盐投加到富含磷酸盐和NH3的污水中,能够形成磷酸铵镁沉淀物,实现污水脱氮除磷。磷酸铵镁水合物(英文简称MAP)俗称鸟粪石,是一种可以缓慢释放的优质肥料。在污水处理厂的各项工艺中,鸟粪石法比较适合应用于厌氧段的溶液中。因为厌氧过程中氮被还原为氨氮,磷被释放出细胞外,所以溶液中氨氮和磷酸根浓度较高。近年来,有许多氮、磷回收技术是基于将鸟粪石法应用于厌氧发酵液、污泥浓缩池中。此外,基于鸟粪石法回收人体尿液中的氮、磷的研究,也受到越来越多的关注。' B" z" S: G: G" u [
, S3 e( U3 t, v6 N+ a饲料和食物蛋白:微生物可以将污水中的无机氮,如NH3和NO3-,经过同化吸收后转化为有机氮,如蛋白质。从耗能的角度来说,污水脱氮和回收氮所消耗的能源是类似的。这项技术的潜在应用领域广泛,例如在水产养殖废水中形成生物絮团供鱼食用、形成可食用的单细胞蛋白等。来源:环保产业,作者:孙晓燕
8 F. u5 S+ p: i5 o- D" d) F& ]
' \; J' }6 O: ?: [7 @6 o |
© 声明:本文仅表作者或发布者个人观点,与环保之家[2TECH.CN]无关。其原创性及陈述文字、内容、数据及图片均未经证实,对本文及其全部或部分内容、图片、文字的真实性、完整性、及时性本站不作任何保证或承诺,仅做参考并自行核实。如有侵权,请联系我们处理,在此深表歉意。
|